¿Podrían haberse reducido las muertes en residencias mediante un estudio del perfil de la microbiota intestinal de los individuos en riesgo y la intervención para recuperar un perfil adecuado?
Un estudio de la London School of Economics con datos de Bélgica, Francia, Irlanda, Noruega, Italia, España y Portugal destaca que entre el 33% y el 64% de las muertes atribuidas a covid-19 en cada país corresponden a residentes de centros de tercera edad1. En España, un 35,8% de los fallecidos vivían en residencias de mayores, pero el porcentaje ascendería al 69% si se incluyeran también los casos con síntomas compatibles de covid-19 (sin confirmación diagnóstica por PCR), según datos del 17 de abril publicados en El País2.
La mortalidad en algunas residencias ha sido devastadora. En Madrid, un 9% de los usuarios habría perdido la vida con la covid-19, un 8% en Navarra y un 4% en Catalunya3. A 17 de abril, la tasa de mortalidad por covid-19 en el conjunto de residencias del Estado ha sido del 1,85% del total de 377.640 residentes2. Un índice de letalidad similar en los casi tres millones de mayores de 75 años que están confinados en sus casas hubiera supuesto 62.355 víctimas solo en esa franja de edad, muy por encima del total de 19.478 muertes registradas en esa fecha. La confinación en una residencia de mayores ha multiplicado por 70 la probabilidad de morir por covid-19 (intervalo de confianza del 95% entre 68 y 72), en comparación con la confinación en casa.
Es posible que vivir confinado en una residencia de mayores haya incrementado el riesgo de contagio, pero lo más preocupante es el elevado índice de mortalidad entre los residentes. La mortalidad sobreviene cuando hay una respuesta inflamatoria descontrolada y la neumonitis progresa tórpidamente a necrosis alveolar masiva, síndrome de distrés respiratorio, sepsis y fallo multiorgánico4. El exceso de mortalidad en las residencias puede estar relacionado con una respuesta inflamatoria inapropiada a la infección por coronavirus. El envejecimiento lleva consigo un deterioro gradual del sistema inmunitario que se define como inmunosenescencia, y se caracteriza por pérdida de la capacidad de generar respuestas inmunitarias adaptativas frente a patógenos no conocidos con anterioridad5. Al no poder recurrir a respuestas inmunitarias especificas frente a nuevos patógenos, la defensa contra el coronavirus en ancianos con inmunosenescencia avanzada consiste en desencadenar una cascada inflamatoria para inactivar al virus, pero la respuesta inflamatoria es perjudicial para las vías respiratorias y sobre todo para tejido alveolar. El enfrentamiento a antígenos no conocidos previamente no es problemático en niños y adultos con capacidad de generar inmunidad adaptativa, pero en la inmunosenescencia puede conducir al fracaso.
La microbiota intestinal juega un papel fundamental en el mantenimiento y equilibrio del sistema inmunitario a lo largo de la vida, y la inmunosenescencia está asociada a deterioro del ecosistema microbiano intestinal. El proyecto ELDERMET demostró que la activación crónica de citoquinas inflamatorias propia de la inmunosenescencia está vinculada a una pérdida de diversidad de la microbiota intestinal, y que esta situación de inflamación persistente (inflammaging) es significativamente más frecuente en personas mayores que viven en centros de larga estancia en comparación con los que viven en la comunidad6. La composición de la microbiota intestinal distinguía claramente a los que vivían en residencias de larga estancia de los que vivían en la comunidad. Ajustando por edad y género, los cambios en composición microbiana se correlacionaban significativamente con un agravamiento de parámetros de inflamación (proteína C reactiva y las citoquinas TNF, IL-6 e IL-8 en plasma) y de fragilidad (presión arterial, exceso de peso, índice Charlson de comorbilidad, Índice de Barthel de discapacidad física, escala de independencia funcional, mini-mental test de Folstein, escala de depresión geriátrica, etc.). La dieta evaluada con cuestionarios de frecuencia de consumo de alimentos también discriminaba entre los grupos, con exceso de proteínas y grasa animal y déficit de vegetales y frutas en las residencias. La pérdida de diversidad de microbiota intestinal (figura 1) podría atribuirse al patrón dietético6, y también al frecuente uso de antibióticos en las residencias7.
Figura 1. Diferencias significativas en la abundancia de géneros bacterianos entre residencias (círculos rojos) y la comunidad (círculos verdes). En la comunidad hay más bacterias fermentadoras y productoras de butirato y en las residencias más proteobacterias (Escherichia/Shigella).
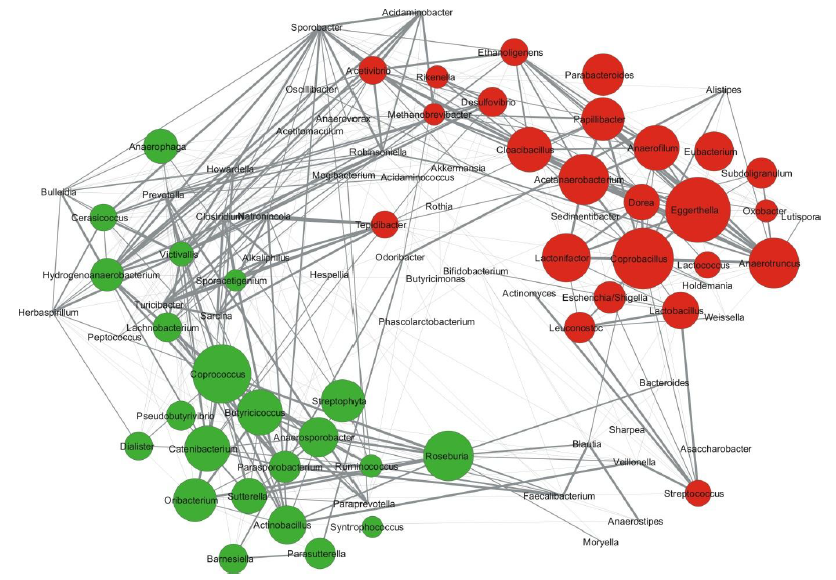
Cabría pensar que el deterioro de la microbiota intestinal en personas que viven en residencias ha acelerado los fenómenos de inmunosenescencia, comprometiendo su capacidad de respuesta frente al coronavirus. Si esto fuera así, la prevención de la disbiosis con dietas más saludables, ricas en frutas y verduras, la limitación del uso de antibióticos, o su uso junto a probióticos adecuados, serían estrategias importantes para evitar los altos índices de mortalidad en las residencias.
Bibliografía
- Comas-Herrera A, Zalakain J, Litwin C, Hsu AT, Fernandez-Plotka J-L. Mortality associated with COVID-19 outbreaks in care homes: early international evidence, 17 April 2020. Article in LTCcovid.org, International Long-Term Care Policy Network, CPEC-LSE.
- Alfageme A, Troya MS, Peinado F. Residencias, la trampa mortal de los más vulnerables. https://elpais.com/sociedad/2020-04-18/residencias-la-trampa-mortal-de-los-mas-vulnerables.html
- Orovio I, Arova JV, Tarin S. Qué ha pasado en las residencias https://www.lavanguardia.com/vida/20200426/48714890909/residencias-mayores-coronavirus.html
- Xu Z, Shi L, Wang Y, Zhang J, Huang L, Zhang C, et al. Pathological findings of COVID-19 associated with acute respiratory distress syndrome. Lancet Respir Med. 2020; 8(4): 420–2.
- Franceschi C, Bonafe M, Valensin S, Olivieri F, de Luca M, Ottaviani E, et al. Inflammaging: An Evolutionary Perspective on Immunosenescence. Ann N Y Acad Sci. 2000; 908(1): 244–54.
- Claesson MJ, Jeffery IB, Conde S, Power SE, O’Connor EM, Cusack S, et al. Gut microbiota composition correlates with diet and health in the elderly. Nature. 2012; 488(7410): 178–84.
- Daneman N, Bronskill SE, Gruneir A, Newman AM, Fischer HD, Rochon PA, et al. Variability in antibiotic use across nursing homes and the risk of antibiotic-related adverse outcomes for individual residents. JAMA Intern Med. 2015; 175(8): 1331–9.



